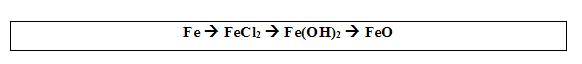Урок по химии «Железо и его свойства»
| (не показаны 3 промежуточные версии 1 участника) | |||
| Строка 68: | Строка 68: | ||
<u>2 группа:</u><br> | <u>2 группа:</u><br> | ||
По распространению в земной коре железо занимает четвертое место среди всех элементов. Минералы: магнитный железняк (магнетит) Fe<sub>3</sub>O<sub>4</sub>; красный железняк (гематит) Fe<sub>2</sub>O<sub>3</sub>, бурый железняк (лимонит) 2Fe<sub>2</sub>O<sub>2</sub> * 3H<sub>2</sub>O; железный или серный колчедан (пирит) FeS<sub>2</sub>.<br> | По распространению в земной коре железо занимает четвертое место среди всех элементов. Минералы: магнитный железняк (магнетит) Fe<sub>3</sub>O<sub>4</sub>; красный железняк (гематит) Fe<sub>2</sub>O<sub>3</sub>, бурый железняк (лимонит) 2Fe<sub>2</sub>O<sub>2</sub> * 3H<sub>2</sub>O; железный или серный колчедан (пирит) FeS<sub>2</sub>.<br> | ||
| − | Задача.<br> | + | ''Задача.'' <br> |
| − | + | ||
{|width=75% | {|width=75% | ||
|Дано: | |Дано: | ||
| − | | | + | | |
|Решение. | |Решение. | ||
|- | |- | ||
| Строка 95: | Строка 94: | ||
|W%<sub>1</sub>(Fe) < W%<sub>2</sub>(Fe) | |W%<sub>1</sub>(Fe) < W%<sub>2</sub>(Fe) | ||
|} | |} | ||
| + | Ответ: минерал магнетит богаче железом <br> | ||
| + | <u>3 группа:</u><br> | ||
| + | Способ получение железного порошка из выданных реактивов – оксида железа (II) и оксида железа(III)<br> | ||
| + | Реактивы: оксид меди (II), цинк, соляная кислота.<br> | ||
| + | a) FeO + 2HCl = FeCl<sub>2</sub> + H<sub>2</sub>O<br> | ||
| + | FeCl<sub>2</sub> + Zn = Fe + ZnCl<sub>2</sub><br> | ||
| + | б) Fe<sub>2</sub>O<sub>3</sub> + 6HCl = 2FeCl<sub>3</sub> + 3H<sub>2</sub>O<br> | ||
| + | 3FeCl<sub>3</sub> + 3Zn = 2Fe + 3ZnCl<sub>2</sub><br> | ||
| + | Проверка его на опыте.<br> | ||
| + | CuO + 2HCl = CuCl<sub>2</sub> + H<sub>2</sub>O<br> | ||
| + | CuCl<sub>2</sub> + Fe = FeCl<sub>2</sub> + Cu <br> | ||
| + | <u>4 группа:</u> <br> | ||
| + | Серебристо-белый блестящий металл, пластичный, ковкий. Обладает свойством намагничиваться и размагничиваться.<br> | ||
| + | '' Задача.''<br> | ||
| + | {| width=75% | ||
| + | |Дано: |||| Решение: | ||
| + | |- | ||
| + | |m(Fe) = 3 г |||| N = NA х m/M = 6 х 1023 х 3/56 = 3,2 х 1022 | ||
| + | |- | ||
| + | | N (Fe) - ?|||| | ||
| + | |- | ||
| + | |} | ||
| + | Ответ: число атомов железа в данном образце 3,2 х 1022<br> | ||
| + | <u>5 и 6 группы:</u><br> | ||
| + | 2Fe0 + 3Cl0<sub>2</sub> = 2Fe+3Cl-3<br> | ||
| + | <center> | ||
| + | [[Изображение:Химическая_формула1.JPG]]<br> | ||
| + | </center> | ||
| + | Fe<sup>0</sup> + S<sup>0</sup> = Fe<sup>+2</sup>S<sup>-2</sup> <br> | ||
| + | 3Fe<sup>0</sup> + 2O<sup>0</sup><sub>2</sub> = <sup>+2</sup>Fe<sup>+3</sup><sub>3</sub>O<sup>-2</sup><sub>4</sub><br> | ||
| + | 3Fe<sup>0</sup> + 4H<sub>2</sub>O = Fe<sub>3</sub>O<sub>4</sub> + 4H<sub>2</sub><br> | ||
| + | Fe<sup>0</sup> + CuSO<sub>4</sub> = Fe+2SO<sub>4</sub> + Cu<br> | ||
| + | Fe<sup>0</sup> + 2HCl = Fe+2Cl<sub>2</sub> + H<sub>2</sub><br> | ||
| + | <center> | ||
| + | [[Изображение:Химическая_формула2.JPG]] | ||
| + | </center> | ||
| + | <u>7 группа:</u><br> | ||
| + | Роль химического элемента железа в жизнедеятельности живых организмов очень велика. Оно входит в состав гемоглобина крови, который осуществляет перенос кислорода от органов дыхания к другим органам и тканям.<br> | ||
| + | Соединения железа издавна применяют для лечения малокровия, при истощении, упадке сил.<br> | ||
| + | '''5. Подведение итогов.''' | ||
| + | Резюме о проделанной работе. | ||
| + | - Сегодня на уроке мы познакомились с новым представителем класса «Металлы» - железом. Рассмотрели его положение в периодической системе Д.И.Менделеева, наблюдали физические, химические свойства и способы получения этого металла, ознакомились с природными минералами и с его значением для жизни.<br> | ||
| + | '''Объявление оценок'''.<br> | ||
| + | '''6.Домашнее задание.'''<br> | ||
| + | Опорный конспект.<br> | ||
| + | |||
| + | |||
| + | |||
| + | |||
Текущая версия на 11:34, 15 июня 2010
Кувшинова Лариса Алексеевна
МОУ лицей № 51 г.о.Тольятти
9 класс
Тип урока: урок формирования новых знаний и умений с использованием групповых форм работы.
Цель урока:
Познакомить учащихся с элементом побочной подгруппы периодической системы Д.И.Менделеева – железом. Рассмотреть физические, химические свойства железа, основные способы его получения, раскрыть биологическое значение железа. Способствовать развитию навыков исследовательской деятельности учащихся, а так же умения аргументировать своё утверждение, воспитывать умение работать в группах.
Оборудование: ПСХЭ Д.И. Менделеева, коллекция «Минералы и горные породы», географическая карта «Полезные ископаемы», компьютер, мультимедийный проектор, экран, лабораторный штатив, прибор для получения газов, магнит, спиртовка, железный стержень, кристаллическая решетка железа (таблица с изображением кристаллической решетки), стакан, электромагнит, аудиокассета, скрепка, микроудобрение, индукционная катушка, провод, картинки с изображением изделий из железа и его сплавов (железнодорожных рельсов, деталей экскаваторов и др.)
Реактивы: оксид меди (II), цинк, соляная кислота, порошкообразное железо, железный гвоздь, вода.
Ход урока.
1. Организационный момент.
2. Вступительное слово учителя. Постановка цели.
- Сегодня мы познакомимся с новым представителем класса «Металлы» - железом.
- Рассмотрим особенности этого элемента в сравнении с ранее изученными металлами.
- Познакомимся с физическими и химическими свойствами этого металла.
- Узнаем о нахождении железа в природе.
- Определим его биологическое значение.
Для работы класс разбивается на 7 групп, каждая группа получает бланк- задание с правом использовать материал учебника, дополнительную информацию и справочную литературу. Время подготовки 10 минут.
- Повторим правила техники безопасности при работе с химическими оборудованием и реактивами и преступаем к работе.
Задание 1-й группы:
«Положение железа в периодической системе химических элементов и строение его атома».
Рассмотреть положение железа в периодической системе химических элементов и строение его атома. Объяснить, на основе каких общих признаков строения атомов элементы побочных подгрупп могут быть объединены в одну группу.
Оборудование: ПСХЭ Д.И. Менделеева.
Задание 2-й группы:
«Нахождение железа в природе».
Из выданных образцов минералов выберите минералы, содержащие железо. Покажите по карте важнейшие месторождения железных руд.
Задача.
Какой из минералов гематит (Fe2O3) или магнетит (Fe3O4) богаче железа? (Решение задачи оформляется на слайдах с помощью мультимедийного проектора, затем во время отчёта проецируется на экран.)
Оборудование: коллекция «Минералы и горные породы», географическая карта «Полезные ископаемы», проектор.
Задание 3-й группы:
«Получение железа».
- В кабинете физики для изучения магнитного поля понадобился порошок железа. Предложите химический способ получение железного порошка из выданных вам реактивов – оксида железа (II) и оксида железа(III)
- и проверьте его на опыте.
Оборудование: лабораторный штатив, прибор для получения газов, спиртовка, магнит.
Реактивы: оксид меди (II), цинк, соляная кислота.
Задание 4-й группы:
«Физические свойства железа».
-Докажите физические свойства железа на примере выданного вам образца.
Задача. Сколько атомов железа содержится в выданном вам образце железа массой 3г.?
Оборудование: Магнит, лабораторный штатив, спиртовка, железный стержень, кристаллическая решетка железа (таблица с изображением кристаллической решетки).
Задание 5-й и 6-й группам:
«Химические свойства железа».
- Мы живём в мире железных конструкций и машин, докажите, огнеопасно ли железо. В атмосфере каких веществ может гореть железо?
Оборудование: Лабораторный штатив, спиртовка, воронка.
Реактивы: Порошкообразное железо.
Методические указания: Проделать опыт самовоспламенения очень мелкого порошка железа с некоторый высоты. Учащиеся должны указать, что в атмосфере кислорода горит компактное железо (в виде листов, балок, проволоки), если предварительно раскалена какая-либо его часть. Привести уравнение реакции горения железа в атмосфере хлора.
Близ города Дели в Индии, стоит железная колонна без малейшего пятнышка ржавчины, хотя её возраст более 2800 лет. Это знаменитая Кутубская колонна высотой около 7 метров и массой 6.5 тонн.
Объясните, почему не происходит ржавление колонны? Всегда ли ржавчина вредна? Как железо реагирует с водяными парами?
Оборудование: стакан.
Реактивы: железо (железный гвоздь), вода.
Задание 7-й группы:
«Применение железа. Значение железа для жизни».
Рассмотреть иллюстрации и выданные приборы. Назовите области их применения. На каком свойстве железа основано их применения?
Оборудование: электромагнит, аудиокассета, скрепка, микроудобрение, индукционная катушка, провод, картинки с изображением изделий из железа и его сплавов (железнодорожных рельсов, деталей экскаваторов и др.)
3. Обмен информацией. Представление работ.
Представители каждый группы представляют отчёт о проделанной работе, а класс принимает участие по обсуждению результатов.
4. Работа в тетрадях. Составление учащимися опорного конспекта.
По мере защиты групп в рабочих тетрадях учащихся должны быть зафиксированы основные выводы, уравнения реакций по каждому из рассматриваемых вопросов.
Опорный конспект:
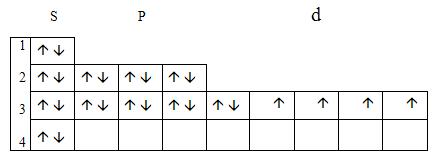
1 группа:
Элемент 8 группы, побочной подгруппы. На последнем энергетическом уровне 2 электрона.
Распределение электронов по уровням: 26Fe 2е;8е;14е;2е
Электронная формула:
1S22S22P63S23P63d64S2
Степень окисления +2 и +3.
2 группа:
По распространению в земной коре железо занимает четвертое место среди всех элементов. Минералы: магнитный железняк (магнетит) Fe3O4; красный железняк (гематит) Fe2O3, бурый железняк (лимонит) 2Fe2O2 * 3H2O; железный или серный колчедан (пирит) FeS2.
Задача.
| Дано: | Решение. | |
| Fe2O3 (гематит) | М(Fe2O3) = 56 * 2 + 16 * 3 = 160 | |
| Fe3O4(магнетит) | W%1(Fe) = 112/160 * 100 = 70% | |
| W%1(Fe) - ? | М(Fe3O4) = 56*3 +16*4 = 232 | |
| W%2(Fe) - ? | W%2(Fe) = 168/232 * 100 = 72,4% | |
| W%1(Fe) < W%2(Fe) |
Ответ: минерал магнетит богаче железом
3 группа:
Способ получение железного порошка из выданных реактивов – оксида железа (II) и оксида железа(III)
Реактивы: оксид меди (II), цинк, соляная кислота.
a) FeO + 2HCl = FeCl2 + H2O
FeCl2 + Zn = Fe + ZnCl2
б) Fe2O3 + 6HCl = 2FeCl3 + 3H2O
3FeCl3 + 3Zn = 2Fe + 3ZnCl2
Проверка его на опыте.
CuO + 2HCl = CuCl2 + H2O
CuCl2 + Fe = FeCl2 + Cu
4 группа:
Серебристо-белый блестящий металл, пластичный, ковкий. Обладает свойством намагничиваться и размагничиваться.
Задача.
| Дано: | Решение: | |
| m(Fe) = 3 г | N = NA х m/M = 6 х 1023 х 3/56 = 3,2 х 1022 | |
| N (Fe) - ? |
Ответ: число атомов железа в данном образце 3,2 х 1022
5 и 6 группы:
2Fe0 + 3Cl02 = 2Fe+3Cl-3
Fe0 + S0 = Fe+2S-2
3Fe0 + 2O02 = +2Fe+33O-24
3Fe0 + 4H2O = Fe3O4 + 4H2
Fe0 + CuSO4 = Fe+2SO4 + Cu
Fe0 + 2HCl = Fe+2Cl2 + H2
7 группа:
Роль химического элемента железа в жизнедеятельности живых организмов очень велика. Оно входит в состав гемоглобина крови, который осуществляет перенос кислорода от органов дыхания к другим органам и тканям.
Соединения железа издавна применяют для лечения малокровия, при истощении, упадке сил.
5. Подведение итогов.
Резюме о проделанной работе.
- Сегодня на уроке мы познакомились с новым представителем класса «Металлы» - железом. Рассмотрели его положение в периодической системе Д.И.Менделеева, наблюдали физические, химические свойства и способы получения этого металла, ознакомились с природными минералами и с его значением для жизни.
Объявление оценок.
6.Домашнее задание.